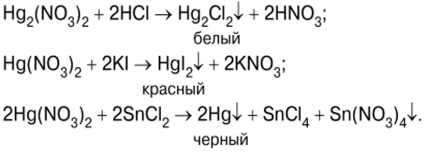
Реакции соединений ртути
Металлическая ртуть и ее соединения высокотоксичны для живых организмов. Особенно это касается соединений, хорошо растворимых в воде. Следует проявлять большую осторожность при экспериментировании с комбинациями этого уникального элемента (ртуть — единственный металл, который находится в жидком состоянии при комнатной температуре). Соблюдение основных заповедей химика? позволит безопасно провести несколько экспериментов с соединениями ртути.
В первом опыте получаем амальгаму алюминия (раствор этого металла в жидкой ртути). Раствор ртути (II) Hg нитрата (V) Hg (NO3)2 и кусок алюминиевой проволоки (фото 1). Алюминиевый стержень (тщательно очищенный от отложений) помещают в пробирку с раствором растворимой соли ртути (фото 2). Через некоторое время мы можем наблюдать выделение пузырьков газа с поверхности проволоки (фото 3 и 4). После извлечения стержня из раствора оказывается, что глина покрыта пушистым налетом, а кроме того, мы видим также шарики металлической ртути (фото 5 и 6).
Химия – опыт соединения ртути
В нормальных условиях поверхность алюминия покрыта плотно прилегающим слоем оксида алюминия.2O3эффективно изолирует металл от агрессивного воздействия окружающей среды. После очистки и погружения стержня в раствор ртутной соли ионы Hg вытесняются2+ более активным алюминием:
Осажденная на поверхности стержня ртуть образует амальгаму с алюминием, что затрудняет прилипание к нему оксида. Алюминий — очень активный металл (реагирует с водой с выделением водорода — наблюдаются пузырьки газа), а его использование в качестве конструкционного материала возможно благодаря плотному оксидному покрытию.
Во втором эксперименте мы обнаружим ионы NH аммония.4+ с помощью реактива Несслера (немецкий химик Юлиус Несслер в 1856 году первым применил его в анализе).
Эксперимент по реакции хмеля и ртутных соединений
Испытание начинается с осаждения иодида ртути (II) HgI.2, после смешивания растворов иодида калия KI и нитрата ртути (II) (V) Hg (NO3)2 (фото 7):
Оранжево-красный осадок HgI2 (фото 8) затем обрабатываем избытком раствора йодида калия до получения растворимого комплексного соединения формулы К2HgI4 ? Тетраиодеркурат калия (II) (Фото 9), который является реактивом Несслера:
С помощью полученного соединения мы можем обнаружить ионы аммония. По-прежнему потребуются растворы гидроксида натрия NaOH и хлорида аммония NH.4Кл (фото 10). После добавления к реактиву Несслера небольшого количества раствора соли аммония и подщелачивания среды сильным основанием наблюдаем образование желто-оранжевой окраски содержимого пробирки. Текущую реакцию можно записать уравнением:
Полученное соединение ртути имеет сложную структуру:
Высокочувствительный тест Несслера используется для обнаружения даже следов солей аммония или аммиака в воде (например, в водопроводной воде).

