Неизвестная периодическая таблица, часть 3
Содержание
Последний эпизод статьи о таблице Менделеева кроме школьной (соответствует названию всей серии). Сегодня об обычно упускаемых из виду группах таблицы Менделеева, искусственных элементах, о которых мы практически ничего не знаем, и о том, что нас ждет в восьмом периоде.
, к двум рядам, обычно помещаемым под доской, в школе относятся пренебрежительно — учитель только упомянет об их существовании и перейдет к другим, «более важным» элементам. Совершенно неадекватные той функции, которую они выполняют в современном мире. Уран i плутон () составляют основу ядерной энергетики: надежный источник в любых климатических условиях (в отличие от нетрадиционной энергетики), а при правильном использовании – безопасный и экологически чистый. Лантаниды в настоящее время являются стратегическим сырьем, необходимым во многих передовых технологиях, например, без лантаноидов не существовало бы современной электроники. Но даже сейчас обе группы трудно взломать по закону периодичности.
Проблема №1: лантаноиды
Менделеев он знал только несколько лантаноидов и без особого труда сумел включить их в таблицу (1). Однако в последующие годы открытия подобных металлов бросили вызов самому закону периодичности. Он требует, чтобы последовательные элементы лежали в соседних группах и имели разные валентности. Между тем лантаноиды с несколько разными атомными массами (а это означало, что они должны были стоять друг за другом в непрерывном ряду) всегда имели валентность, равную III (некоторые еще и II или IV), т. е. находились в одной группе. Было выдвинуто множество теорий о лантаноиды, например, все они считались одним и тем же элементом в разных вариантах. Проблему решили, поместив лантаноиды в один «ящик» системы, но только квантовая механика 20-х и 30-х годов объяснила их положение в периодической таблице.
1. Церий, наиболее распространенный лантанид. Все остальные лантаноиды аналогичны и похожи на алюминий ()
Проблема с лантаноидами актуальна и сегодня. На самом деле неизвестно, с какого элемента они начинаются и заканчиваются. Согласно большинству учебников, лантан, хотя и дал название всему семейству, к нему не относится – это скандальный из группы 3лантаноиды – это металлы от церия до лютеция. Однако противоположные мнения указывают на то, что последний член семьи гораздо лучше сканирует. молиться. Его физические свойства и химическая природа образующихся соединений лучше соответствуют свойствам других элементов группы 3 (таким образом, лантаноиды – это металлы от лантана до иттербия). Дискуссии между химиками продолжаются до сих пор, а авторы книг по-разному представляют местонахождение этих элементов (2).
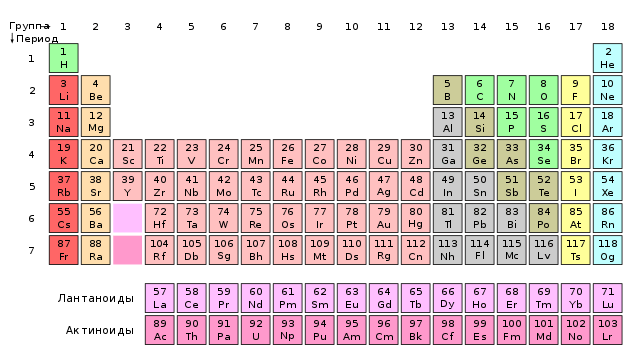
2. Самая длинная форма таблицы Менделеева. Лантаниды и актиниды начинаются сразу после группы 2, а скандлеры включают лютеций и лоренс.
Проблема №2: актиниды
актиниды, то есть элементы от актиния до лоренса, составляют группу, аналогичную лантаноидам, помещенную в следующий период. Проблема с актинидами была и остается такой же, как и с лантаноидами. Менделеев знал только две актиниды и без труда перечислил их в таблице (3). Tor с наиболее прочной валентностью группа IV досталась группе титана и циркония, а группа VI со значением уран встречается в компании хрома, молибдена и вольфрама.
Открытия рубежа XNUMX и XNUMX веков потрясли систему: появилось дюжина или около того радиоактивных элементов. Некоторые из них имели одинаковые массы, но разные свойства, а другие имели одинаковые свойства — разные массы. Этот факт противоречил предыдущим знаниям, но открытие изотопов прояснило некоторые проблемы. Большинство элементов оказались смесями атомов с разной массой (но, конечно, с одинаковым числом протонов в ядре). Возвращаясь к актиноидам, два из них появились в начале прошлого века. Актиний сразу оказался сходным с лантаном (его радиоактивность была обнаружена в осадках лантаноидов, осажденных из растворов, содержащих актиний), а протактиний попал в группу с ванадием, ниобием и танталом как V-ценный элемент. До 40-х годов первые четыре актиноида спокойно располагались в группах с 3 по 6.
3. Наиболее распространенные актиноиды: слева торий, покрытый слоем двуокиси, справа уран ()
Проблема возникла во время реализации Манхэттенского проекта. Физики и химики были уверены, что произвели элементы тяжелее уранаоднако не смогли обнаружить их присутствие химическими средствами. Например: элемент 93 рядом с ураном не вел себя как представитель группы 7. Это было только предположение Глена Сиборга, более позднего первооткрывателя нескольких трансурановых элементов, что элементы, начинающиеся с актиния, образуют ряды, аналогичные лантаноидам, решенные проблема (4). Применение разработанных методов разделения лантаноидов, главным образом хроматографии, позволило в последующие годы идентифицировать искусственные элементы. О совершенстве техники и мастерстве экспериментаторов свидетельствует тот факт, что наличие некоторых новых элементов было обнаружено всего с десятком их атомов! (5).
Но не верьте, что торий или уран вдруг изменили свои свойства и стали лантаноидоподобными, трехвалентными металлами. Они по-прежнему имеют больше общего с титанидами и хромами, чем с другими актинидами. Аналогично с протактинатами и даже некоторыми трансуранистами. Об определенном сходстве можно говорить только во второй половине серии. Однако нельзя сказать, что лантаноиды и актиниды являются родственными семействами (как будто их расположение в периодической таблице предполагает их местонахождение).
4. Гленн Сиборг (1912-99) указывает символ элемента, названного в его честь.
5. Родина многих трансуранистов — циклотрон Национальной лаборатории Лоуренса в Беркли (август 1939 г.)
Нет экспериментальных данных
Неточное знание свойств наиболее тяжелых трансуранидов связано с недостаточным количеством материала для исследований. Последним элементом, который производится в заметном количестве миллиграммов, является эйнштейн, занимающий 99-е место в таблице. Конечно, проводятся опыты и с другими трансуранидами, но в их случае, например, исследуется характерное излучение, возникающее в осадке, и не наблюдается образования кристаллов соединений.
Физико-химические свойства нельзя просто измерить, а только оценить по косвенным наблюдениям. Аналогичная проблема возникает с двумя более легкими элементами: астату (№ 85) я франсу (№ 87). Из-за малого времени жизни их видимые количества еще не получены, и теория должна заполнить пробелы в наблюдениях и измерениях. С другой стороны, ежегодное производство плутония, который обнаруживается в следовых количествах в земной коре, составляет несколько тонн и лучше изучено, чем многие более легкие стойкие элементы.
Еще большая проблема связана с самыми тяжелыми элементами с периодом 7 после актинидов. В их случае приходится оперировать буквально отдельными атомами, время жизни которых исчисляется долями секунды. Больше невозможно определить радиоактивность, присутствующую в осадке соединения, связанного с элементом, а только исследовать некоторые физические свойства (например, скорость осаждения на данной поверхности) и, таким образом, сделать выводы о химическом сходстве. Конечно, помогает теория, точнее расчеты, основанные на квантовой механике. Однако результаты не на 100% достоверны, например, по определенному распределению электронов на оболочках еще далеко до описания химических свойств. Чем дальше мы удаляемся от непосредственных наблюдательных данных, тем более ненадежным становится вывод «методом Менделеева» (то есть на основе свойств известных элементов).
Химики и физики пытаются предсказать свойства даже самых тяжелых, еще не полученных элементов следующего периода. Элементы 119 и 120, вероятно, будут иметь черты, мало чем отличающиеся от расположенных выше франции и радия (в группах 1 и 2 изменение физико-химических свойств вполне закономерно). В периоде 8, подобно лантаноидам и актиноидам, будет целых 18 очень похожих свойств элементов g-блока, с которыми ученые еще не занимались.
Расчеты предполагают существование в этот период элементов с валентностью до 12. Вероятно, в системе окажется элемент 164, у более тяжелых заряд ядра будет настолько велик, что на них будут падать электроны, а скорость движения по орбитам превысила бы скорость света. Проведенные расчеты не дают однозначных результатов, некоторые сдвигают границы таблицы Менделеева примерно на десяток элементов.
Закон периодичности на помойку?
Прочитав статью, вы, вероятно, пришли к выводу, что большое количество исключений из правил, данных в школе, это дает вам право ответить на вопрос утвердительно. Но не давайте его слишком быстро. Закон периодичности он сформулирован очень обобщенно (свойства периодически повторяются), что является одновременно его преимуществом и недостатком. Преимущество, ведь действительно, анализируя положение элемента в таблице, построенной на основе закона, можно сделать выводы о его физико-химических свойствах. Недостаток, так как выводы часто оказываются неточными или даже ложными.
Закон периодичности хорошо работает в основных группах (1, 2, 13-18), лучше в их верхних частях, чем в нижних. Прекрасным примером является период 3: от натрия к аргону валентность и химические свойства меняются регулярно без каких-либо неожиданностей. В боковых группах (3-12) отклонения уже хорошо видны, но о проблемах с лантаноидами и актинидами вы читали выше. В общем, чем дальше от начала системы, тем менее точно выполняется закон периодичности.
Так в мусорку? Вселенная химических элементов и отношения, которые они создают, представляют собой систему настолько сложную, что даже гениальная идея Менделеева не может охватить ее целиком. Закон, безусловно, нуждается в корректировке и уточнении. Если сравнить Менделеева с Ньютоном (поскольку и закон периодичности, и теория тяготения организовали и объяснили большие куски окружающего мира), можно сделать вывод, что химики все еще ждут своего Эйнштейна.
Смотрите также:

