
Химическая (?) Нобелевская премия 2014 г.
Содержание
Начало октября – время, когда в мире науки царит атмосфера лихорадочного ожидания. В этот период Шведская королевская академия наук и Каролинский институт присуждают Нобелевские премии по физике, химии и медицине. 10 октября 2014 г. было объявлено, что 106-я премия по химии была присуждена Эрику Бетцигу, Стефану Хеллу и Уильяму Мёрнеру «за их вклад в развитие флуоресцентной микроскопии высокого разрешения». В обоснование было добавлено, что благодаря работе ученых «микроскопия стала «наноскопией»».
«Юный техник», опубликовав в ноябрьском номере статьи о полемике вокруг Нобелевской премии, проявил большую дальновидность (на момент подготовки текстов приговор этого года еще не был известен). Различие в химии вызвало большое удивление у химиков — и не только у них. Неудивительно, что награду получили несколько ученых, ведь в настоящее время совместные исследования проводятся международными коллективами из учреждений, расположенных даже в разных уголках мира.
Неудивительно и то, что «химическая» Нобелевская премия все реже присуждается за типовые работы в этой области, а в последние годы она стала скорее «биохимической» наградой. Вы уже привыкли к этому. Но награда за микроскоп?! По единодушному мнению, это отличие вполне заслужено, но гораздо лучше оно соответствовало бы Нобелевской премии по физике, потому что флуоресцентный микроскоп — это оптический прибор. Возможно — медицина, потому что в основном они используются для изучения мельчайших деталей клеточного строения.
Оптический микроскоп и его ограничения
В 1677 году голландский натуралист Антони ван Левенгук сконструировал первый микроскопкоторые можно было бы использовать в исследованиях. Хотя микроскопы были построены в конце прошлого века, только конструкция Левенгука была пригодна для практического использования. Исследователи увидели мир, о котором они раньше не подозревали, — вселенную микроскопических существ и клеток, из которых строятся более крупные организмы.
Изобретение оказалось очень полезным, поэтому над его развитием велась интенсивная работа. В 1873 веке оптические микроскопы (изучаемый объект освещался видимым светом) были почти совершенны, когда барьер был реализован законами природы. В 400 году немецкий физик Эрнст Аббе доказал, что две точки на изображении можно увидеть, если расстояние между ними примерно больше половины длины волны света, используемого для наблюдения. В противном случае они сливаются вместе. Поскольку человек еще может воспринимать фиолетовый свет с длиной волны 200 нм, это означает, что практически невозможно различить две точки, находящиеся на расстоянии менее 1 нм (10 нм = 9-4 м). Многие клеточные структуры, не говоря уже о молекулах белков и нуклеиновых кислот, намного меньше по размеру (XNUMX). Есть микроскопы (электронные, атомно-силовые), позволяющие получить гораздо лучшее разрешение (видны даже очертания отдельных атомов), но они не годятся для наблюдения живых клеток и процессов, происходящих в них.
4. Сравнение размеров некоторых объектов (слева: муравей, волосы, клетка млекопитающего, бактерии, митохондрии,
вирус, белковая частица, многоатомная частица). Предел разрешения оптического микроскопа отмечен (1 мкм = 1000 нм). (© Нобель Медиа АБ)
Светящиеся молекулы
Молекулы химических соединений поглощают электромагнитное излучение, а затем излучают его в окружающую среду. В некоторых случаях часть энергии рассеивается в виде тепла, а остальная часть излучается в виде света с большей длиной волны, чем поглощаемая. Это явление называется флуоресценцией (от плавикового шпата CaF2, в кристаллах которого оно впервые наблюдалось). Некоторые из соединений, присутствующих в клетках, также флуоресцируют (например, хлорофилл), который использовался в конструкции флуоресцентного микроскопа. Так стало возможным увидеть некоторые компоненты клетки, которые трудно разглядеть при обычном освещении.
В 60-е годы так называемая зеленый флуоресцентный белок (GFP). Он нетоксичен и легко модифицируется химическим путем. Были получены белки, которые светятся несколькими цветами и могут присоединяться к разным молекулам. Благодаря этим достижениям удалось получить флуоресцентные изображения расположения испытуемых соединений (других белков, нуклеиновых кислот) в клетке. Однако по-прежнему действовал «запрет Аббе» — детали менее 200 нм различить было нельзя.
В 1989 году Уильям Э. Мёрнер впервые получил изображение одиночной светящейся молекулы. (молекулы находились на расстоянии более 200 нм друг от друга). Правда, это явление наблюдалось в сильно разбавленных газах гораздо раньше, но ученый сделал это в растворе, т.е. в среде обитания клеток (5). В 1997 г. Мёрнер, модифицировав GFP, получил белок, который при облучении излучением соответствующей длины волны мог включаться (тогда флуоресцентный) или выключаться (не флуоресцентный).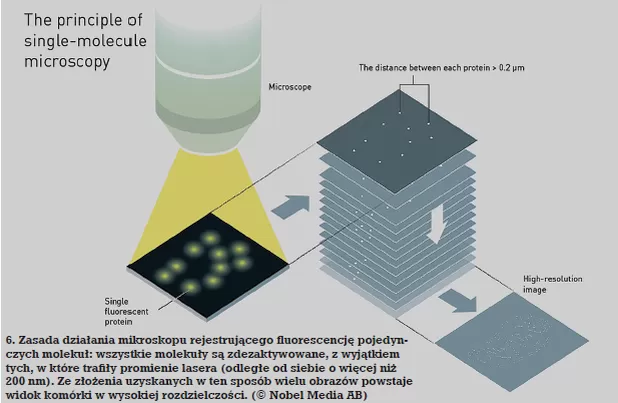
Наложение картинок друг на друга
7. Сравнение разрешающей способности обыкновенного
флуоресцентный микроскоп и микроскоп STED
Открытие Мёрнера решило проблему, поставленную двумя годами ранее Эрика Бетцига. Он предложил использовать светящиеся молекулы в разных цветах и рассредоточены в клетке на расстоянии более 200 нм друг от друга. Заставляя молекулы флуоресцировать определенным цветом, можно было точно определить их положение и, таким образом, местоположение связанных клеточных фрагментов. Это позволило бы достичь разрешения лучше предела 200 нм. К сожалению, таких молекул в то время не было.
В 2006 году Бетциг и его команда сконструировали флуоресцентный микроскоп, в котором использовались световые частицы не разного цвета, а такие, которые можно было включать и выключать по желанию. Метод заключается в следующем: ячейку с введенными внутрь флуоресцирующими молекулами освещают излучением, подобранным таким образом, чтобы все молекулы были дезактивированы. Затем на него воздействуют одиночными лазерными импульсами, удаленными друг от друга более чем на 200 нм, которые возбуждают молекулы до флуоресценции.
Затем все молекулы снова выключаются, а другие молекулы стимулируются к тому, чтобы сиять, чем раньше. В результате наложения множества полученных таким образом спектров (разумеется, с использованием достаточно мощного компьютера) получается изображение клетки, на котором можно различить детали, отстоящие друг от друга всего на десяток или около того нм ( 6). Вариации этого метода называются: PALM (микроскопия фотоактивированной локализации — микроскопия фотоактивационной локализации), БУРЯ (микроскопия стохастической оптической реконструкции — микроскопия случайной реконструкции изображения) или ПОКРАСИТЬ (накопление точек для визуализации в наноразмерной топографии — накопление точек для визуализации в наноразмерной топографии).
Сузьте поле зрения
Шнобелевская премия 2014 г.
В этом году работы химиков не были отмечены жюри
наград (это случилось уже в третий раз за ее 24-летнюю
уже история). Некоторые из высоко оцененных достижений
химическое «послевкусие» (этот термин, вероятно, не
на месте…) имеет отличие в области питания.
Испанские ученые отделили от содержимого младенцев
подгузники (!) молочнокислые бактерии, которые затем
используется для производства созревшего мяса. Позвольте нам напомнить вам
что японские исследователи были отмечены семью годами ранее,
получивший ванильный аромат коровьих «пирожков».
Пожалуй, не стоит — ради собственного аппетита
— изучить все кухонные секреты…?
Третий лауреат Нобелевской премии Стефан В. Хелл тоже думал о преодолении границы в 200 нм. Уже в 1994 году он предложил следующее решение: одним лазерным импульсом надо стимулировать флуоресцентные молекулы в поле зрения, а следующим (в форме бублика) — излучать излучение, выключая таким образом все, кроме находящихся в круг диаметром примерно 20 нм. Таким образом, изображение будет содержать светящуюся точку в центре поля зрения (или не будет, если флуоресцирующей молекулы в данный момент там не было). Затем микроскоп перемещают к следующему месту клетки и вся процедура повторяется.
Компьютерная система управляет всей точной механикой, что позволяет очень точно (от этого зависит достоверность полученного изображения) определить местоположение аппарата. Таким образом, сканируя всю клетку, можно получить ее изображение с разрешением до дюжины или около того нм (7). Флуоресцентный микроскоп, работающий по этому принципу, был построен компанией Hella в 2000 году, и этот метод называется STED (стимулированное эмиссионное истощение) (8).
И где во всем этом химия?
9. Ядро клетки опухоли кости: изображение слева
в обычном флуоресцентном микроскопе, правильно
– w микроскопия PALM
Где именно? Попробуем найти ответ на этот вопрос.
Прежде всего: границы между классическими научными дисциплинами давно размыты, и исследователи наиболее успешны в где встречаются разные поля. Поэтому ученый, изучающий живые клетки, должен быть и биологом, и химиком, и физиком, не забывая при этом о прекрасном знании работы вычислительной техники и сложной исследовательской аппаратуры.
Во-вторых: отмеченные наградами микроскопические методы позируют огромное поле для химиков покрасоваться. По мере их развития потребуются новые флуоресцентные молекулы, которые будут избирательно связываться с выбранными компонентами клетки (и кто-то должен синтезировать соответствующие молекулы). Если работа химиков будет успешной, можно представить себе гораздо лучшую диагностику различных заболеваний и расширение знаний о функционировании нашего организма (9).
Третье и последнее: в следующем месяце мы представим на MT флуоресценция в домашней лаборатории.
8. Принцип работы STED-микроскопа
(слева классический микроскоп, в котором образец освещается
лазерный луч): 1) на образец падает лазерный луч, который стимулирует молекулы к флуоресценции (синий цвет)
и луч, гасящий их свечение (оранжевое) в пределах поля зрения (кроме центра);
2) микроскоп скользит по поверхности образца; 3) получаем готовое изображение в высоком разрешении.
(© Нобель Медиа АБ)
